L-glutamin v buněčných kulturách
L-glutamin je běžný bezsérový doplněk stravy používaný v aplikacích biomanufacturingu, tkáňového inženýrství, speciálních buněčných kulturách, jako je kultivace hybridomů, a dalších běžných aplikacích kultivace savčích buněk. Protože je však l-glutamin nestabilní esenciální aminokyselina, většina komerčně dostupných médií má složení s volným L-glutaminem zahrnutým v základním složení nebo se přidává do tekutých přípravků v době použití.
Nabízíme glutamin pro buněčné kultury jako dipeptid nebo proteinový hydrolyzát. Některá patentovaná média používaná v biomanuální výrobě jsou doplněna L-glutaminem v dipeptidové formě, jako je alanyl-l-glutamin a glycyl-l-glutamin. Méně definovaným zdrojem L-glutaminu jsou bílkovinné hydrolyzáty, zejména hydrolyzáty lepku. Pro potřeby médií bez séra nebo živočišných bílkovin, jako je kultivace rekombinantních buněk vaječníků čínského křečka (rCHO), je pšeničný lepek bohatým zdrojem peptidylglutaminu.
Přečtěte si více informací o
Produkty
Jako doplněk v klasických médiích pro buněčné kultury se používá koncentrace L-glutaminu v rozmezí od 0,5 mM v Amesově médiu do 10 mM v MCDB médiu 131. Typičtější koncentrace v těchto médiích pro aplikace v oblasti biomanufacturingu a tkáňového inženýrství se pohybuje mezi 2 a 4 mM.
Optimální koncentrace L-glutaminu v DMEM/F12 Nutrient Mixture je 2.5 mM, zatímco v médiu Hybridoma Medium bez séra a bílkovin je to 2,7 mM. U DMEM je GMEM, IMDM a H-Y médium, optimální koncentrace je 4 mM. IMDM se často používá jako výchozí složení pro patentovaná média pro kultivaci hybridomových buněk; hybridomové buňky rostou lépe v koncentracích L-glutaminu, které jsou vyšší než průměrné hladiny zjištěné v médiích.
L-glutamin v systémech pro buněčné kultury
Vzhledem k jeho chemické nestabilitě a významu pro růst a funkci buněk je velmi důležité, aby dodávka L-glutaminu byla optimalizována pro každý jedinečný proces buněčné kultury. Glutamin má molekulový vzorec C5H10N2O3 a molekulovou hmotnost 146,15 g/mol, izoelektrický bod 5,65 a pka 2,17 a 9,13. V případě, že je glutamin v roztoku, je jeho molekulová hmotnost nižší než molekulová hmotnost. Pochopení tohoto chemického složení a rozmanitých forem dodávání L-glutaminu a jeho alternativ je nezbytné pro efektivní použití tohoto doplňku v aplikacích buněčných kultur.
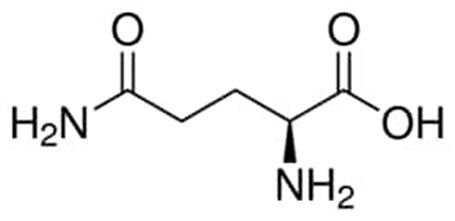
Obrázek 1.Chemická struktura L-glutaminu.
Glutamin podporuje růst buněk, které mají vysoké energetické nároky a syntetizují velké množství bílkovin a nukleových kyselin. Je také alternativním zdrojem energie pro rychle se dělící buňky a buňky, které glukózu využívají neefektivně. Buňky potřebují atomy dusíku obsažené v glutaminu ke stavbě molekul, jako jsou nukleotidy, aminokyseliny, aminocukry a vitaminy.
Glutamin je prekurzorem glutamátu, klíčové aminokyseliny používané pro transaminaci alfa ketokyselin za vzniku dalších alfa aminokyselin. Obsahuje jeden atom dusíku jako amid a druhý atom dusíku jako amin; také přenáší a dodává dusík do buněk v množství, které není tak toxické jako volný amoniak.
Pokud je hladina glukózy nízká a energetické nároky vysoké, mohou buňky metabolizovat aminokyseliny pro získání energie. Amidový dusík glutaminu se využívá při syntéze vitaminů NAD a NADP, purinových nukleotidů, CTP z UTP a asparaginu. Dusík původně uložený v glutaminu může být také použit k výrobě karbamylfosfátu pro syntézu pyrimidinů. Glutamin je jednou z nejsnáze dostupných aminokyselin pro použití jako zdroj energie a je hlavním zdrojem energie pro mnoho rychle se dělících typů buněk in vitro.
Stabilita glutaminu v médiích buněčných kultur
Pokud je glutamin přítomen jako aminokyselinový zbytek v proteinech nebo peptidech, je stabilní. Podmíněně esenciální aminokyselina je volně rozpustná neutrální aminokyselina obsahující amid R-skupiny. Protože je nestabilní, může se v kapalném prostředí neenzymaticky rozkládat na amoniak a pyroglutamát (pyrolidonkarboxylovou kyselinu). Rozklad L-glutaminu v průběhu času závisí na pH, teplotě a přítomnosti různých aniontů.
Deaminace glutaminu, což je reakce, při které se odstraňuje aminoskupina, probíhá jak v kyselých, tak v zásaditých podmínkách. Reakce probíhá výrazně rychleji v přítomnosti fosforečnanů nebo hydrogenuhličitanů v médiu. Při fixní koncentraci fosfátů v kapalném médiu se rychlost deaminace zvyšuje se zvýšením pH z 4,3 na 10.
Biochemie L-glutaminu
Reakce, které fixují dusík na glutamát a glutamin, spotřebovávají energetické ekvivalenty, jako je NADH, NADPH nebo ATP. Glutamát je syntetizován z amoniaku a kyseliny alfa ketoglutarinové, meziproduktu cyklu trikarboxylové kyseliny (TCA). Tato syntéza vyžaduje oxidaci NADH nebo NADPH. Enzymy podílející se na syntéze glutamátu, glutamátdehydrogenáza (EC 1.4.1.4) a glutamátsyntáza (EC 1.4.1.13), jsou reverzibilní.
Amonium, anorganický zdroj dusíku využívaný buňkami, se zpočátku začleňuje do organického dusíku jako amin glutamátu nebo amid glutamátu. Tyto dvě aminokyseliny představují primární zásobárnu dusíku pro syntézu bílkovin, nukleových kyselin a dalších dusíkatých sloučenin. Amonium produkované in vivo, ale ne in vitro, může být metabolizováno na močovinu. Za některých podmínek in vitro se amoniak hromadí v extracelulárním prostředí jako amonný ion.
Glutamin je syntetizován z molekul amoniaku a glutamátu. Při této syntéze se spotřebovává energie ve formě ATP. Enzym zodpovědný za tuto syntézu, glutamin syntetáza (EC 6.3.1.2), je vysoce regulován, aby omezil produkci glutaminu na požadavky buňky. Katabolismus glutaminu na glutamát a amonium je zprostředkován mitochondriálními enzymy zvanými glutaminázy (EC 3.5.1.2).
Abyste mohli pokračovat ve čtení, přihlaste se nebo vytvořte účet.
Nemáte účet?