Auftragsdienstleistungen für mRNA & LNP

Beschleunigte Entwicklung von mRNA-basierten Impfstoffen und Therapeutika zur Deckung des Behandlungsbedarfs der Patienten
Mit unserem Leistungsangebot Millipore® CTDMO-Services bereiten wir den Weg für robuste, integrierte und konsistente Prozesse in sämtlichen Phasen – von der Präklinik bis zur Marktreife. Die Kombination aus Kompetenzen, fachlicher Expertise und regulatorischem Fachwissen unterstützt unsere Kunden beim Erreichen ihrer Ziele – um mRNA-basierte Impfstoffe und Therapeutika schneller auf den Markt zu bringen und für das Leben von Patienten Entscheidendes zu bewirken.
Das Angebotsspektrum unserer Millipore® CTDMO-Services umfasst kundenspezifische Dienstleistungen zur Beschleunigung von Projekten, Risikominderung und Verkürzung der Time-to-Market – von mRNA über Lipide und Lipid-Nanopartikel (LNP) bis hin zum Fill & Finish.
Unsere Leistungsbilanz
20+
Jahre Erfahrung bei der erfolgreichen Herstellung von mRNA, Lipiden und LNP
10.000
-fach geringere Menge pDNA benötigt dank PCR-basierter mRNA-Herstellung der nächsten Generation
50+
erfolgreiche Einzelprojekte zur Synthese von Lipiden
6
kommerzielle Arzneimittel hergestellt
6+
hochgradig vernetzte Standorte, die Geschwindigkeit, Skalierbarkeit, Qualität und Flexibilität sicherstellen

Präklinische Phase
Unsere Fachexperten stehen Ihnen vom ersten Konzept über die mRNA-Synthese, kundenspezifische Lipide sowie das Screening und die Optimierung von Lipid-Nanopartikel-Formulierungen für Nukleinsäure-Payloads zur Seite.

Klinische Prüfung
Der Technologietransfer und die Skalierbarkeit des Prozesses für die GMP-konforme Herstellung von klinischem Prüfmaterial sind von entscheidender Bedeutung. Mit den Millipore® CTDMO-Services unterstützt Sie unser Team dabei, Ihr Entwicklungsprogramm für mRNA-LNP-basierte Wirkstoffe zu skalieren und in die klinische Prüfung zu überführen. Im Fokus stehen dabei die Prozesseffizienz und Einhaltung regulatorischer Anforderungen.

Kommerzielle Herstellung
Die Einhaltung von GMP-Standards in Bezug auf Herstellung, Qualität, Sicherheit und Wirksamkeit ist für mRNA-LNP-basierte Therapeutika und Impfstoffe auf dem Weg zur Vermarktung zwingend erforderlich. Unsere Experten verhelfen Kunden zu der nötigen Geschwindigkeit, indem sie sie bei der Risikobewertung und dem Risikomanagement unterstützen und die Einhaltung von Qualitätsanforderungen sicherstellen, mit dem Ziel, die Markteinführung zu beschleunigen.
Unser Angebot

mRNA
Wir sind auf die Herstellung vollständig kundenspezifischer funktioneller mRNA spezialisiert und bieten umfassende fachliche und technische Unterstützung vom Projektdesign über die Sequenzoptimierung bis hin zu Daten für Dossiers für neue Prüfpräparate (IND). Mit unserem bewährten PCR-basierten Workflow ist die mRNA-Herstellung in hohem Maße reproduzierbar und das Endprodukt weist überragende Eigenschaften auf.
- PCR-basiertes Verfahren der nächsten Generation für qualitativ hochwertige mRNA
- Vollkommen kundenspezifische mRNA-Herstellung
- Präklinischer bis GMP-konformer kommerzieller Maßstab – von mg bis kg*
* Die Verfahrens- und analytische Entwicklung von GMP-Projekten können wir im Q3 2023 aufnehmen. Transfer in GMP-konforme Produktionsanlagen im Q1 2024.

Lipide
Wir sind hochspezialisiert auf die Synthese hochwertiger GMP-konformer Lipide für pharmazeutische Anwendungen und Gentherapien und konzentrieren uns auf die maßgeschneiderte Herstellung gemäß der Anforderungen unserer.
- Hochwertige Syntheseprodukte
- Flexibilität dank maßgeschneidertem Angebot und Standardsortiment
- GMP-konforme Lipide vom Klein- bis Großmaßstab – in Mengen von Gramm bis Tonnen

Lipid-Nanopartikel (LNP)
Mit unseren Millipore® CTDMO Services unterstützen wir Pioniere dabei, ihre APIs (mRNA, siRNA, cas9RNA etc.) bis zu den Patienten zu bringen. Dank unserer 20-jährigen Erfahrung in der Herstellung für die präklinische Entwicklung, die klinische Prüfung und den kommerziellen Bedarf verhelfen wir den Projekten unserer Kunden zum Erfolg.
- Formulierungsentwicklung durch Hochdurchsatz-Screening aus mehreren Lipidbibliotheken und Prozessoptimierung
- Interner Transfer zu GMP
- Präklinischer bis GMP-konformer kommerzieller Maßstab – von Milliliter-Mengen bis hin zu mehreren hundert Litern
- Interner Transfer von LNP-Herstellung bis hin zum Fill & Finish
- Chargengrößen < 1–1.200 l

Analyseentwicklung & Qualitätskontrolle
Angesichts der einzigartigen Eigenschaften des mRNA/LNP-Komplexes sind neue Erkenntnisse und neuartige Analysemöglichkeiten erforderlich, um schnell bereitstehende, wirksame und gesetzeskonforme mRNA-basierte Impfstoffe und Arzneimittel zu ermöglichen. Unsere Prüfdienstleistungen für mRNA-Ausgangsstoffe, Arzneimittelwirkstoffe und Arzneimittelprodukte umfassen:
- Reinheit und produktbezogene Verunreinigungen
- Sicherheit
- Stärke, Identität und Potenz
- Produktcharakterisierung und Qualität
- Arzneibuchbasierte Prüfung
Globale Präsenz
Wir sind ein einziges Unternehmen mit einem globalen Netzwerk, das CDMO-Services in allen Phasen der Wertschöpfungskette von Molekülen anbietet.
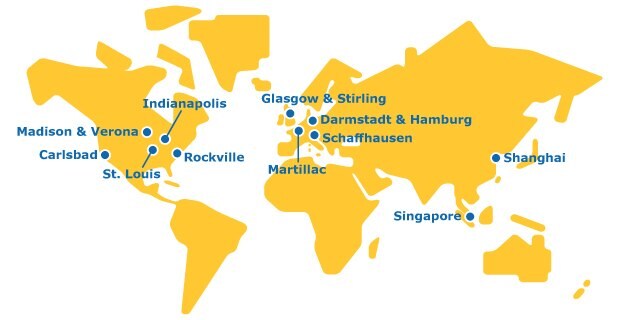
Ein hochgradig vernetztes CDMO-Netzwerk, um Geschwindigkeit, Skalierbarkeit, Qualität und Flexibilität für die Herstellung von mRNA, Lipiden und LNP sicherzustellen.

Unser Exzellenzzentrum für mRNA der späten klinischen und kommerziellen Phase, Produktionsstandorte für unsere Portfolio-Lipide, einschließlich Lipidproduktion in großem Maßstab und Formulierungs-Screening-Dienste in der frühen Phase

Unser Exzellenzzentrum für mRNA der frühen klinischen Phase

Unser Exzellenzzentrum, das auf die Synthese von hochwertigen Portfolio- und kundenspezifischen Lipiden spezialisiert ist

Unser Exzellenzzentrum für die Herstellung von Lipidnanopartikeln (inkl. Fill & Finish)

Produktionsstandort für Portfolio- und kundenspezifische Lipide sowie Prozessentwicklung für Liposome und LNP

Unsere Biosicherheitsprüfungen und Herstellungsdienstleistungen umfassen den gesamten Produktzyklus von der frühen präklinischen Entwicklung bis zur Produktion unter Lizenz. Das Dienstleistungsspektrum umfasst analytische Entwicklung, Erstellung von Zellbanken, Charakterisierung von Zelllinien, Virusabreicherung, Freigabeprüfung von Wirkstoffen und Fertigarzneimitteln sowie Schnellmethoden.
Zugehörige technische Informationen
- Strategies for Successful Formulation Development of Lipid-Based RNA Delivery and Vaccines
Here, we explore lipid-based RNA therapeutic development, specifically application opportunities and the performance-defining parameters.
Externe Informationsquellen
- Successful Drug Development with Synthetic Lipids - Critical Aspects and Strategies
Learn more about the essential aspects and strategies of successful drug development and commercialization of lipid-based drug products.
Um weiterzulesen, melden Sie sich bitte an oder erstellen ein Konto.
Sie haben kein Konto?