C–H官能基化
C–H官能基化は、有機合成化学における究極の反応法とされてきました。1近年、有機化学、有機金属、および触媒化学の分野で、C–H結合の反応性の解明とそれを利用した堅牢な反応開発が大きな進歩を遂げており、これらの方法論を逆合成の一般的な手法の一つとして広く活用できる段階に来ているといえるでしょう。2-11 C–H結合をC–C、C–N、C–O、またはC–X結合に選択的かつ精密に制御された方法で確実に変換する手法は、ステップエコノミーと廃棄物削減の観点から有益です。
注目のカテゴリー
お客様の研究を推進するために必要な基本構成要素を、メルクの有機ビルディングブロックのポートフォリオで見つけてください。アルケン、アルカン、アルキン、アレーン、アレンなど。
複素環ビルディングブロックは、化学者が有機合成のために使用する構造フラグメントグループの中で最も大規模で多様なファミリーです。メルクは複素環ビルディングブロックを網羅した包括的ポートフォリオをお届けします。
トリフルオロメチル、ジフルオロメチル、トリフラート、ペンタフルオロスルファニルなどの含フッ素ビルディングブロックを豊富に取り揃え、お客様のツールボックスへ提供することにより、目的化合物により簡単にたどりつけるようサポートします。
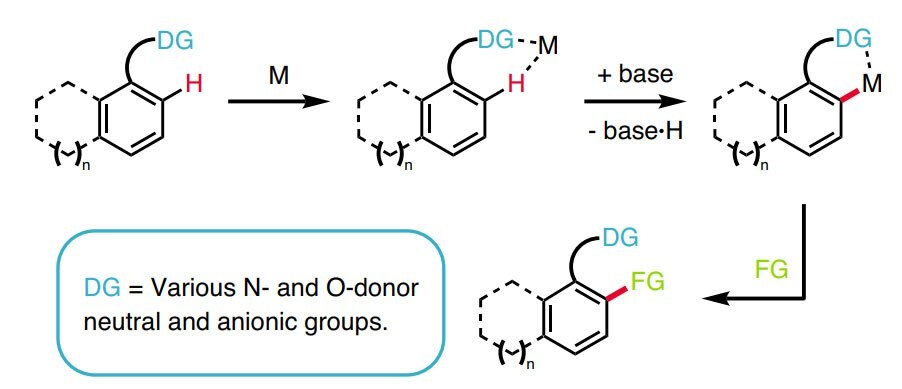
C–H活性化反応は、特定の分子において反応ターゲットにできるサイトの選択肢を増やし、より複雑な化合物合成のチャンスを増やします。さらに、従来とは完全に異なる化学結合をターゲットにできる高度な化学選択性を備えている点が特徴です。従来の官能基反応と組み合わせることで、C-H官能基化は、複雑な天然物や医薬品合成を大幅に合理化します。C-H官能基化を合成手法の一つに適用することは明らかに利点がありますが、12有機化学の多くのカリキュラムでは、この手法を積極的に活用するようにはまだ更新されていません。詳細は、C-H官能基化反応マニュアルを参照してください。
関連資料
- Professor Karl Anker Jørgensen and his group have developed ethers which serve as excellent chiral organocatalysts in the direct asymmetric α-functionalization of aldehydes.
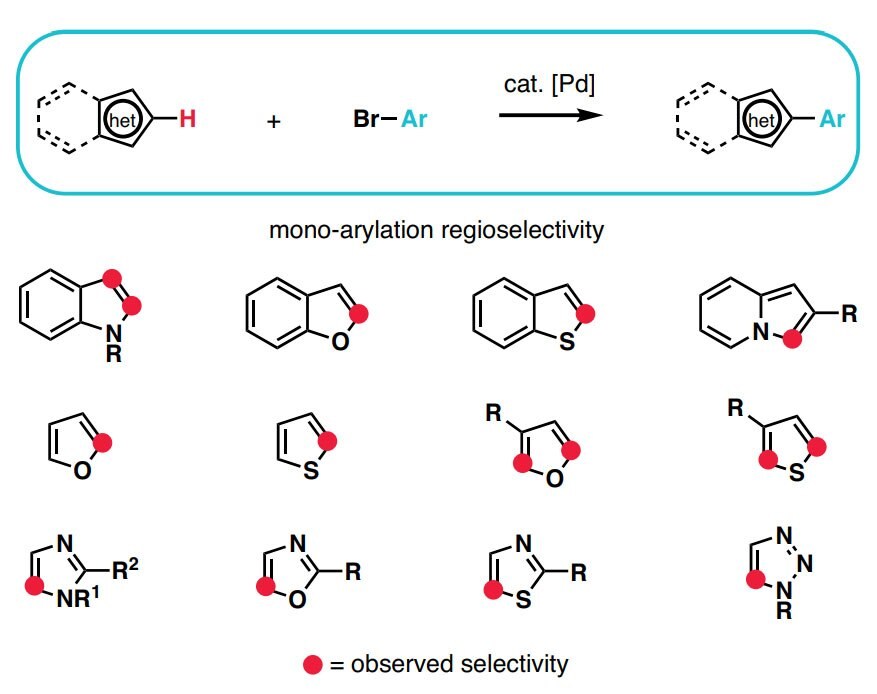
- 芳香族および芳香族ヘテロ環化合物の合成は、化学工業の中核となるテーマです。新しい分子構造への要求がますます増加する中で、どの研究プロジェクトにおいてもコストの削減や開発のスピードアップが求められており、芳香族(ヘテロ環)骨格を多様化する迅速な手法が必要とされています。
- The Du Bois group at Stanford University has made substantial progress within the field of Rh-catalyzed C–H amination via oxidative cyclization of carbamate, sulfamate, sulfamide, urea, and guanidine substrates to give 1,2- and 1,3-heteroatom motifs masked in the form of 5- and 6-membered ring heterocycles.
- 塩化アリールはクロスカップリング反応に利用される化合物であり、医薬品候補化合物や天然物の合成において重要な中間体です。
- 水の存在下でのC-H活性化反応とそれに伴うC-C結合形成のための、リサイクル可能でリガンドを必要としないルテニウム触媒
- すべて表示 (15)
関連プロトコル
- 発色剤を用いた明視野解析と蛍光顕微鏡法を用いたFFPEおよび凍結組織を利用した免疫組織染色(IHC)プロトコルのトラブルシューティング:うまくいくコツ
- すべて表示 (0)
お問い合わせ
ご不明な点がございましたら、お問い合わせページをご覧いただくか
、テクニカルサービスまでお問い合わせください。
メール:jpts@merckgroup.com
電話:03-6756-8245
サポート
- Chromatogram Search
Use the Chromatogram Search to identify unknown compounds in your sample.
- 計算ツール・アプリ
ウェブツールボックス-分析化学、ライフサイエンス、化学合成および材料科学のためのサイエンスリサーチツールとリソース
- Customer Support Request
お問い合わせページでは、製品のお問い合わせや、注文や納期、お取引やアカウント、ウェブサイトに関するお問い合わせをお申込みいただけます。
- FAQ
Explore our Frequently Asked Questions for answers to commonly asked questions about our products and services.
参考文献
続きを確認するには、ログインするか、新規登録が必要です。
アカウントをお持ちではありませんか?