Biofarmáciai jellemzés

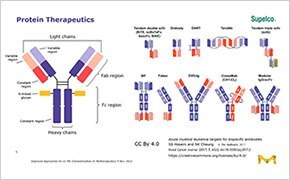
A biofarmakonok biotechnológiai módszerekkel előállított gyógyszerek. Ide tartoznak a monoklonális antitestek (mAbs), a terápiás fehérjék, a fúziós fehérjék, az antitest-gyógyszer konjugátumok és más hasonló biológiai készítmények. A jellemzési vizsgálatok a biofarmáciai anyagok fizikai és kémiai tulajdonságainak megértését jelentik. A gyógyszerfejlesztés során ezek a tulajdonságok hatással lehetnek a termék teljesítményére, feldolgozhatóságára, stabilitására és megjelenésére.
Kiemelt kategóriák
Pontos elválasztásokat érhet el széles HPLC-oszlopgyűjteményünkkel. Növelje a visszatartást, a felbontást és a szelektivitást. Rendeljen még ma.
Tekintse meg fejlett sejttenyésztő eszközeink kínálatát a kutatás, a gyógyszerkutatás és a gyártás számára. A táptalajtól a tenyésztőeszközökig mindenre felkészültünk.
Böngésszen a fehérje-, enzim- és kismolekulás termékek között a sejtbiológiai, tenyésztés-kiegészítő és útvonal-vizsgálatokhoz.
Böngésszen a fehérje-, enzim- és kismolekulás termékek között a sejtbiológiai, tenyésztés-kiegészítő és útvonal-vizsgálatokhoz.
Biológiai gyógyszerek, biohasonló készítmények jellemzése és elemzése
A biológiai gyógyszerek elemzéséhez és jellemzéséhez rendkívül kifinomult analitikai munkafolyamatokra van szükség, amelyek jelentős hangsúlyt fektetnek a GMP és a jogszabályi megfelelésre. Mind egy eredeti bioterápia, mind egy biohasonló fejlesztése termékkarakterizációs vizsgálatokat igényel a robusztus és jól specifikált biológiai gyógyszer biztosítása érdekében.
Identitás
Intact tömeg meghatározása
Az intakt molekulatömeg meghatározása, amelyet gyakran SEC-MS és megfelelő standardok segítségével végeznek, szükséges lépés a biológiai gyógyszerek jellemzésében, a klónok kiválasztásától a végtermék ellenőrzéséig. Az intakt molekulatömeg-elemzést általában a fehérje/peptidtermékek sokféleségének kimutatására és a biotermékek azonosságának igazolására használják. Optimalizálással az összes fehérjetermék intakt molekulatömegét is meg lehet határozni, beleértve a bispecifikus monoklonális antitesteket is.
Ahelyett, hogy egy nagy fehérje biotermék nehézkes intakt tömegével kellene foglalkozni, egy fehérje emésztéses analízis megközelítést alkalmaznak, ahol a mintát először csak néhány fragmentumra hasítják, majd az elválasztás után a szétválasztás egyedileg kezelhető speciális tömegspektrométeres proteomikai standardokkal.
Titermérés
A sejtvonal termelékenysége a megfelelő mennyiségű mAb előállítására, befolyásolja annak kereskedelmi potenciálját. Az alapszintű mérésként használt titer mérése Protein-A affinitáskromatográfiával (HPLC) történik. A mAb fejlesztése során kezdetben nagyszámú terméssejtkultúra (HCC) mintát kellett szűrni IgG-titer szempontjából. Affinitás kromatográfiát Protein-A ligandumot alkalmazva gyakran használják a mAb koncentrációjának meghatározására, valamint tisztítására a downstream aggregátum- és töltésváltozat-elemzéshez.
Aminosav-analízis
Aminosav-analízis a termékazonosság megállapításának népszerű módja, és a mAb aminosav-összetételének meghatározására használják. Gyakran végzik az extinkciós együttható mérésével együtt, amely a különböző gyártmányok közötti titer megállapítására rutinszerűen alkalmazott módszer.
A metrológiailag érvényes eljárásokkal kijelölt értékekkel rendelkező hitelesített referenciaanyagok kritikus fontosságúak lesznek az aminosav-analízis munkafolyamatának minden lépése során, beleértve a fehérjeextrakciót, frakcionálást, dúsítást, proteolízist és elemzést, a kísérleti eltérések minimalizálása és ellenőrzése érdekében.
Peptidtérképezés
A mAb azonosságának megállapításához elegendő lehet az egyszerű, egyetlen enzimet tartalmazó peptidtérképek összehasonlítása. A részletesebb terápiás antitest jellemzés, beleértve az N- vagy C-terminális szekvenálást, a glikánok jellemzését, valamint az antitestgyártás, -elemzés, -tisztítás és -fragmentálás egyéb szempontjait, jobban tájékoztathat a terméktervezésről. Proteomikai tömegspektrometria további szerkezeti információkat nyújt.
Poszt-transzlációs módosítás
N-glikánelemzés
A nagymértékben változó glikoziláció hatással lehet a mAb tisztaságára és változó funkciót eredményezhet. A monoklonális antitestek N-glikánokat hordoznak a gerincükön, amelyek LC-MS segítségével felszabadíthatók a glikozilációs mintázatok értékeléséhez. A monoklonális antitestek N-glikánjainak jellemzése szükséges, hogy a vizsgált molekula teljes szerkezeti részleteit megismerjük. Ezeknek az N-glikán útvonalaknak a megértése azért fontos, mert az N-glikánok a glikoproteinek számos tulajdonságát befolyásolják, beleértve a glikánok konformációját, oldhatóságát, antigenitását és glikánkötő fehérjék általi felismerését.
Monoklonális antitestek (mAb-k) magasabb rendű szerkezetének (HOS) összehasonlítása
A HOS-t - a mAb 3D szerkezetét - számos tényező befolyásolja, kezdve a mAb előállításához használt sejtvonal kiválasztásától a biológiai feldolgozási körülményekig, mint például a hőmérséklet, a pH és a fényexpozíció. A hidrogén-deutériumcsere tömegspektrometria (HDX-MS) egy olyan módszer, amelyet a mAb tercier szerkezetének részletes megismerésére alkalmaznak.
mAb módosítások elemzése
A mAb gyártási folyamat során számos különböző poszttranszlációs módosítás történhet, amelyeket nagyban befolyásolnak az olyan folyamatparaméterek, mint a közeg, a hőmérséklet stb. A konzisztens termék előállítása érdekében kritikus fontosságú, hogy ezeket a módosításokat a mAb szintézis minden egyes fordulója során reprodukáljuk. Modifikációs elemzés magában foglalja a diszulfidhidak feltérképezését és a glikán alapszerkezetének értékelését. A szialilációt is célszerű számszerűsíteni, mivel a szialinsav negatív hatással lehet a mAb-re.
mAb töltéseloszlás
A poszttranszlációs módosítások (PTM) vagy kémiai módosítások eredményeként a töltésváltozatok jelentős hatással lehetnek a mAb biológiai aktivitására és farmakokinetikájára. A mAb-kre vonatkozó szabályozási követelmény, a töltésváltozatok elemzése olyan technikákkal értékelhető, mint a kationcserés kromatográfia (CEX) és a kapilláris izoelektromos fókuszálás (cIEF).
mAb Fizikai vizsgálat és méreteloszlás
mAb fizikai vizsgálata
A fizikai vizsgálat a mAb megjelenésének jellemzésére szolgál, például a pH, az ozmolalitás és a koncentráció mérése. A csomagolás integritását is értékelik a fizikai vizsgálati protokollon belül, például Karl Fischer-féle nedvességelemzéssel vagy festék bejutásával a zárás integritásának megerősítésére.
HmAb méreteloszlás
Míg az egységes mAb termék kívánatos, a kezdeti gyártási anyag gyakran tartalmaz méretváltozatokat, például aggregátumokat, fragmentumokat és további könnyű láncokat mutató biomolekulákat. Mivel ezek potenciálisan befolyásolhatják az immunogenitást és a hatékonyságot, fontos jelenlétük nyomon követése. A méretkizárásos kromatográfia (SEC) a leggyakrabban használt módszer a méreteloszlás értékelésére.
Szilárdság és szennyeződések
Host-cell protein szennyeződések
.A bioterápiákban PPM-szinten jelenlévő gazdasejtfehérje (HCP) szennyeződések jelentős immunogenitási kockázatot jelentenek, mivel kiszámíthatatlan immunválaszt válthatnak ki a betegekben. Összetett és változatos természetük miatt nehéz kimutatni vagy nyomon követni őket. Míg a legtöbb HCP szennyeződés hatékonyan eltávolítható a tipikus tisztítási folyamatok során, a HCP-k egy kis populációja különösen nagy kihívást jelent. Egy nehezen eltávolítható CHO HCP, a lipoprotein lipáz koppintását fejlesztették ki a monoklonális antitest formulákban a poliszorbát stabilitásának javítása érdekében.
Gyártási adalékanyagok ellenőrzése
A mAb-fejlesztés és -gyártás során a gyártási adalékanyagok széles skáláját kell ellenőrizni, beleértve Tisztítószerek, Protein A, Transzfekciós reagensek, antibiotikumok, habzásgátlók és növekedési faktorok.
mAbs mikrobiológiai vizsgálatok
A GMP és a GMP-nek megfelelő gyógyszerfejlesztéshez és -gyártáshoz számos mikrobiológiai vizsgálati eljárás szükséges. Számos mAb-t mikroorganizmusokban állítanak elő, hogy kihasználják gyors növekedési sebességüket és nagy hozamukat, ezért kritikus fontosságú a mikrobiális szennyeződések jelenlétének nyomon követése és ellenőrzése. A Gram-negatív baktériumok sejtfalának endotoxinnak nevezett összetevője a láztól és hidegrázástól a halálos szeptikus sokkig terjedő reakciókat vált ki, ami a pyrogén kimutatását (MAT in vitro tesztelés) és az azt követő eltávolítását a mAb-ból kulcsfontosságúvá és szabályozási követelménnyé teszi. Bioburden tesztelést kell alkalmazni a teljes mAb gyártási folyamat során a potenciálisan káros mikrobiális szennyeződések jelenlétének ellenőrzésére. Sterilitásvizsgálat szintén kritikus a mAb gyártás integritásának megerősítéséhez.
Látogasson el dokumentumkeresőnkbe adatlapok, tanúsítványok és műszaki dokumentációk kereséséhez.
Kapcsolódó műszaki cikkek
- A complete SEC-UV workflow for the characterization of mAb monomers, aggregates, and fragments using Zenix® and Zenix®-C SEC columns, including system suitability testing and forced pH and temperature stress studies.
- Optimization of a Reversed-Phase Liquid Chromatographic (RP-LC) method for the intact analysis of a therapeutic monoclonal antibody, trastuzumab, using a BIOshell™ A400 Protein C4 column.
- Explore various strategies for deglycosylating N-linked glycans involving PNGase F, PNGase A (Glycopeptidase A), and even native and sequential deglycosylation with endoglycosidases like Endoglycosidase H, Endoglycosidase F, and exoglycosidases.
- Comparative analysis of different columns in resolving medium-sized fragments of monoclonal antibodies, after digestion using dithiothreitol (DTT) or IdeS (a protease), by Reversed-Phase Chromatography.
- Step-by-step workflows for the intact mass analysis, peptide mapping, and N-glycan analysis of the monoclonal antibody― adalimumab, for an accurate characterization of the critical quality attributes (CQAs) to ensure drug safety and efficacy. Read more.
- Mindent látni (17)
Kapcsolódó protokollok
- An optimized LC-MS/MS based workflow for low artifact tryptic digestion and peptide mapping of monoclonal antibody, adalimumab (Humira) using filter assisted sample preparation (FASP).
- A step-by-step protocol for released N-linked glycan analysis of the monoclonal antibody adalimumab, based on UHPLC-FLR-MS and procainamide labeling.
- A complete workflow for the intact and middle-up mass analysis of reduced and non-reduced monoclonal antibodies based on SEC-MS with sample preparation by protein-A affinity clean-up.
- BIOshell™ IgG 1000 Å C4 UHPLC Column for Improved Biomacromolecule Separations
- SigmaMab Antibody Drug Conjugate Mimic, is a non-toxic drug mimic utilized as a standard for mass spectrometry and high performance liquid chromatography.
- Mindent látni (5)
További cikkek és protokollok keresése
Kapcsolódó webináriumok
Ez a webinárium a mAb-k intakt és középső elemzésére vonatkozó alapvető kromatográfiás megközelítéseket tárgyalja, mielőtt részletesebb és összetettebb elemzési stratégiákba bocsátkoznánk.
Webinárium: Tippek a jobb peptidtérképezéshez
Ez a webinárium a monoklonális antitestek "alulról felfelé" történő elemzésének fejlődését tárgyalja, miközben kiemeli az oszlopkémia szerepét és fontosságát a peptidek nagy szelektivitású, nagy teljesítményű folyadékkromatográfiás (HPLC) módszereinek fejlesztésében.
A webinárium a peptidek "alulról felfelé" történő elemzését tárgyalja.Ez a webinárium azt mutatja be, hogyan lehet innovatív módszerekkel javítani a bioterápiás karakterizáció precizitásának megértését.
Hogyan tudunk segíteni
Kérdés esetén kérjük, küldjön ügyféltámogatási kérelmet
vagy beszéljen ügyfélszolgálatunkkal:
Emailt küldjön custserv@sial.com
vagy hívja a +1 (800) 244-1173-as telefonszámot
További támogatás
- Chromatogram Search
Use the Chromatogram Search to identify unknown compounds in your sample.
- Számológépek és alkalmazások
Web Toolbox - tudományos kutatási eszközök és források az analitikai kémia, az élettudomány, a kémiai szintézis és az anyagtudomány számára.
- Customer Support Request
Customer support including help with orders, products, accounts, and website technical issues.
- FAQ
Explore our Frequently Asked Questions for answers to commonly asked questions about our products and services.
Az olvasás folytatásához jelentkezzen be vagy hozzon létre egy felhasználói fiókot.
Még nem rendelkezik fiókkal?